重大进展!华东理工大学杨弋/陈显军首次对RNA功能和代谢进行光遗传学控制
RNA 结合蛋白 (RBP) 在调节细胞环境中 RNA 的功能方面发挥着重要作用,但在时间和空间上控制 RBP 活动的能力是有限的。
2022年1月3日,华东理工大学杨弋及陈显军共同通讯在Nature Biotechnology 在线发表题为“Optogenetic control of RNA function and metabolism using engineered light-switchable RNA-binding proteins ”的研究论文,该研究描述了 LicV 的工程,LicV 是一种光开关 RBP,它结合特定的 RNA 序列以响应蓝光照射。
当与各种 RNA 效应器融合时,LicV 允许对细胞培养中的 RNA 定位、剪接、翻译和稳定性进行光遗传学控制。此外,LicV 辅助的 CRISPR-Cas 系统允许对转录和基因组位点标记进行有效和可调的光开关调节。这些数据表明,可光控 RBP LicV 可作为可编程支架用于合成 RNA 效应器的时空控制。

最近的研究重塑了关于 RNA 功能的先前概念,特别是在多种细胞活动中发挥重要作用的众多非编码 RNA。RNA在细胞内的特定时间和位置表现出复杂的动力学和功能,这些动力学包括其表达、降解、易位、剪接和其他化学修饰的变化;因此,能够精确和时空操纵 RNA 动力学和功能的技术对于理解活细胞中 RNA 的生理功能非常需要。为此,光是一种理想的触发器,因为它很容易获得、高度可调、无毒,最重要的是,它具有很高的时空分辨率。
一些研究试图通过使用紫外线激活化学笼状的 RNA 来控制 RNA 的功能。这些努力允许对基因表达、核酶活性、CRISPR-Cas 功能和蛋白质-RNA 交联 进行光学控制。然而,生物学家对这些方法的接受程度有限,可能是因为紫外线辐射的毒性以及与笼式 RNA 合成相关的技术复杂性。或者,RNA 功能可能由遗传编码的光开关 RBPs光遗传控制。
光遗传学是一种新兴技术,在该技术中,基因编码的光开关蛋白用于操纵生物过程,具有无与伦比的灵活性和高时空精度。在真核细胞中,许多蛋白质被认为具有 RBP 的功能,几乎控制着 RNA 代谢的所有方面,包括转录、加工、翻译、周转和细胞定位。然而,关于自然光可切换 RBP 的报道极为罕见。
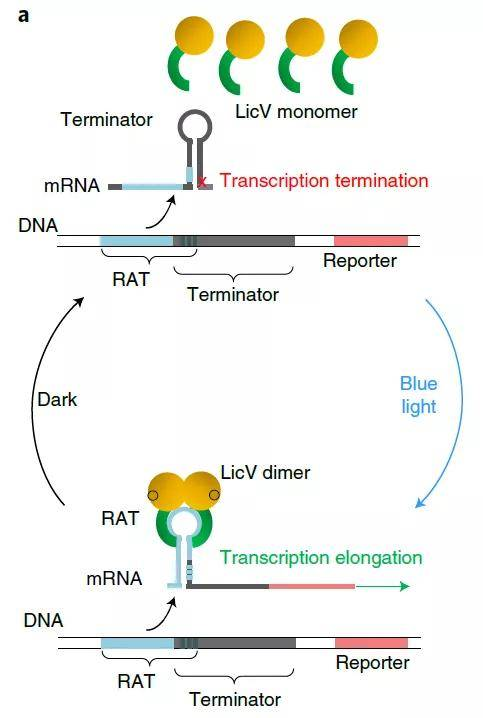
工程光控 RBP(图源自Nature Biotechnology )
最近,Weber 等人选择了一种 RNA 适配体,它可以以依赖光的方式特异性结合天然蓝光受体 PAL。光激活的 PAL-RNA 相互作用被证明能够在细菌和哺乳动物细胞中进行翻译抑制。研究人员假设合成光开关 RBP 也可以由天然 RBP 和光感受器设计而成。以前,开发了几种光控 DNA 结合蛋白 (DBP) 和光遗传学转录控制系统,用于利用光对基因转录进行可逆、可调和时空调控,其中,出现了受一个光控 DBP 控制的单组分系统因其简单的优点和大的开/关比而受到青睐。
这些光开关 DBP 基于简单的模块化设计,由 DNA 结合域和包含小光氧电压 (LOV) 域的蛋白质组成。暴露于蓝光后,光开关 DBP 的寡聚化状态和结合能力会改变为其同源 DNA 序列的寡聚化状态和结合能力,这直接导致基因转录激活或抑制。因此,研究人员假设用 RNA 结合基序替换光可开关 DBP 中的 DNA 结合基序将产生光可开关 RBP,这可能是用于 RNA 生物学研究的有价值的光遗传学工具。该研究描述了 LicV 的工程,LicV 是一种光开关 RBP,它结合特定的 RNA 序列以响应蓝光照射。
当与各种 RNA 效应器融合时,LicV 允许对细胞培养中的 RNA 定位、剪接、翻译和稳定性进行光遗传学控制。此外,LicV 辅助的 CRISPR-Cas 系统允许对转录和基因组位点标记进行有效和可调的光开关调节。这些数据表明,可光控 RBP LicV 可作为可编程支架用于合成 RNA 效应器的时空控制。